Die Fähigkeit unseres Organismus, Körperfremdes zu erkennen sowie schnell und hochspezifisch abzuwehren, haben wir soeben kennengelernt. Es liegt nahe anzunehmen, daß jedes Individuum die Immunantwort in gleicher Weise bewerkstelligt. Dies ist aber offensichtlich nicht der Fall. Die individuelle genetische Ausstattung der Lebewesen gestattet es den einzelnen Individuen in z.T. sehr unterschiedlicher Art und Weise auf ihre Umwelt zu reagieren. Dazu müssen zwei Voraussetzungen erfüllt sein. Erstens, die Möglichkeit, daß ein „Fremdstoff“ in einen Organismus eindringen und sein „Opfer“ erreichen kann und zweitens die Fähigkeit des Individuums, sich mit dem Eindringling wirksam auseinanderzusetzen, ihn zu neutralisieren und zu eliminieren.
Möglicherweise hat die unterschiedliche Empfänglichkeit (Suszeptibilität) einzelner Individuen gegenüber bestimmten Krankheitskeimen oder Noxen (Umweltgiften) einen ähnlichen genetischen Hintergrund wie die unterschiedliche individuelle Reaktivität gegenüber dem gleichen Agens. Vielleicht sind es nur zwei Seiten einer Medaille. So ist man bestrebt, herauszufinden, über welchen molekularen Mechanismus dieses Phänomen zu erklären sei. Es gibt zwei prinzipielle Ansätze, sich der Lösung zu nähern. Beide erklären sich über den molekularen Polymorphismus. Ersterer gründet sich auf dem Fehlen der Synthese bestimmter passender Liganden („Andockstellen“) für einzelne Keime auf der Zelloberfläche des Wirtes, ein zweiter auf der An- oder Abwesenheit von Genprodukten bestimmter individueller enzymkodierender Allele. Beide Lösungswege sehen die Ursachen individueller Suszeptibilität in der genetischen Ausstattung.
Zu den wohl spektakulärsten Erkenntnissen auf diesem Gebiet gehört die Entdeckung einer der Ursachen für das Ausbleiben einer HIV-Infektion bei bestimmten Personen trotz eines hohen Infektionsrisikos durch häufigen Kontakt mit nachweislich HIV-seropositiven und erkrankten Sexualpartnern. Auf dem Chromosom 3 befindet sich ein Gen (CCR5), das in mehreren allelen Formen bei verschiedenen Individuen vorkommt. Eines der Allele (CCR5-D32), das bei etwa 10 Prozent der deutschen Bevölkerung anzutreffen ist, beeinflußt in starkem Maße das Voranschreiten der HIV-Erkrankung. Personen, die von beiden Eltern das Allel CCR5-D32 geerbt haben, also für dieses Allel homozygot sind, sind in der Regel vor einer HIV-Infektion geschützt. Anders dagegen diejenigen, die dieses Allel nur von einem Elterteil geerbt haben. Bei ihnen verzögert sich nur der Ausbruch des Vollbildes der Erkrankung um einige Jahre, verglichen mit Personen, die das Allel nicht geerbt haben. Das Gen kodiert die Synthese eines Rezeptors für chemische Botenstoffe (Chemokine) in der Zellmembran der T-Lymphozyten. Bei diesem Rezeptor handelt es sich um eine der Andockstellen des HI-Virus. Daher bildet dieser Rezeptor auch einen der pharmakologischen Ansatzpunkte zur Behandlung der Immunschwächekrankheit.
Umfangreiche Studien an Inzuchtmäusen haben gezeigt, daß es einen allgemeinen genetischen Hintergrund für die Stärke und Effektivität der Immunantwort geben muß. Inzuchtmäuse eignen sich für solche Experimente besonders gut, weil durch Kreuzen mit einem genetisch definierten Mäusestamm und ständiges Rückkreuzen der Geschwistertiere über mehr als 10 Generationen Tierkolonien mit einem definierten Erbgut entstehen. Auf diese Weise konnten Mäusestämme mit unterschiedlicher Immunreaktivität gezüchtet werden. Sie werden entsprechend ihrer schwachen oder starken Reaktivität gegen verschiedene Antigene als Low-(oder Non-) und High-Responder bezeichnet. Dieses unterschiedliche Verhalten konnte in umfangreichen Analysen sogenannten Immunresponse(Immunantwort)-Genen zugeordnet und die Vererbbarkeit dieser Eigenschaften nachgewiesen werden. Solche Immunresponsgene sind auch für den Menschen beschrieben worden. Sie gehören zum Haupthistokompatikomplex (MHC) und sind für eine erfolgreiche Organtransplantation von entscheidender Bedeutung, wobei die Ursache für die unterschiedliche Reaktivität offensichtlich auf der Ebene der Regulation der Antigenpräsentation im Rahmen der spezifischen Antigenerkennung liegt.
Bereits in der zweiten Hälfte des 19. Jahrhunderts gab es Beobachtungen, die darauf hinwiesen, daß genetische Faktoren die Bereitschaft zu einer Krankheit beeinflussen. Die Beobachtung, daß es ein familiär gehäuftes Auftreten von Diphtherie gibt, führte zu der Vermutung, daß Resistenz oder Empfindlichkeit eines Individuums gegen das Diphtheriebakterium zu reagieren, ein angeborenes Merkmal sein könnte. Diese Vermutung wurde durch die Entdeckung gestützt, daß verschiedene Stämme von Meerschweinchen unterschiedliche Resistenzmuster gegen Diphtherie ausbilden und daß die Bildung von Antikörpern gegen das Diphtherietoxin durch ein Gen kontrolliert wird, das nach den Mendelschen Regeln dominant vererbt wird.
In der klinischen Praxis gibt es Erfahrungen, die auf einen ähnlichen Zusammenhang zwischen individueller genetischer Ausstattung und Immunreaktivität hinweisen. Da sind an erster Stelle die sogenannten „Impfversager“ zu nennen. Dabei handelt es sich um Personen, die nach einer aktiven Impfung nachweislich (z.B. Antikörperbildung) nur schwach oder gar nicht gegen den Impfstoff reagieren. (Die Natur ist in dieser Hinsicht allerdings auch nicht hundertprozentig perfekt, d.h., nach „natürlichen“ Infektionen kann man auch ein weiteres Mal erkranken.) In der Regel ist der Prozentsatz an Low- und Nonrespondern gering (unter 10%), der Zusammenhang zwischen Reaktivität und genetischen Faktoren für einige Krankheitserreger (Hepatitis B, Diphtherie und Tetanus, Haemophilus influenzae, Bordatella (Keuchhusten)ist jedoch nachgewiesen.
Dialysepatienten leiden aufgrund gestörter Blutbildung häufig an einem Mangel an roten Blutkörperchen, der heutzutage durch die Gabe des durch die Dopingskandale bekanntgewordenen gentechnisch hergestellten Hormons Erytropoeitin erfolgreich behandelt werden kann und die Verabreichung von Blutkonserven in vielen Fällen überflüssig macht. Es gab jedoch Zeiten, als die Gabe von Bluttransfusionen noch sehr liberal gehandhabt wurde. So auch für die genannten Dialysepatienten. Neben der Gefahr, durch die Blutübertragung Infektionserreger zu übertragen, bestand für die potentiellen Transplantatempfänger das Risiko, durch den Anteil an weißen Blutkörperchen in der Blutkonserve immunisiert zu werden. Wie wir wissen, sind Letztere – insbesondere die Lymphozyten – Träger der Transplantationsantigene. Sie können in einem fremden Individuum – also dem Dialysepatienten – eine Immunantwort auslösen und zu langlebigen antigenspezifischen Gedächtniszellen führen, denn bei der Transfusion wird in der Regel nur auf die Blutgruppe der roten Blutkörperchen geachtet. Für den Dialysepatienten kann das fatale Folgen haben.
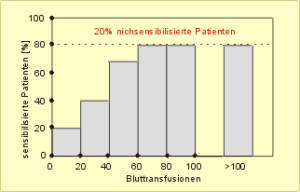
In diesem Zusammenhang werteten wir bei fast eintausend Dialysepatienten den Zusammenhang zwischen dem Auftreten von Antikörpern (Sensibilisierung) gegen Lymphozyten und der Anzahl verabreichter Bluttransfusionen aus. Es zeigte sich, daß mit steigender Zahl an Bluttransfusionen der Anteil sensibilisierter – also immunisierter – Patienten kontinuierlich zunimmt. Doch nach sechzig Transfusionen gab es keinen weiteren Anstieg (Abb. 42). Selbst nach mehr als einhundert (in einigen Fällen über zweihundert) Transfusionen blieb es bei einer Immunisierungsrate von etwa 80% der Patienten. Über die restlichen 20% nichtimmunisierter Patienten kann man spekulieren. Unsere erste Vermutung war, daß es sich um Personen handelt, die man aufgrund ihrer genetischen Ausstattung als Low- oder Nonresponder bezeichnen könnte. Allerdings sind andere Erklärungen ebenfalls möglich.
Die unterschiedliche Fähigkeit, auf fremde Moleküle aus der Umwelt zu reagieren, ist nicht allein auf die genetische Ausstattung eines Individuums zurückzuführen. Sie kann auch im Laufe des Lebens erworben werden. Wir haben das Phänomen des immunologischen Gedächtnisses schon mehrfach erwähnt. Nach der ersten Auseinandersetzung des Organismus mit fremden Molekülen bleiben spezifische Immunzellen zurück, die bei einem weiteren Kontakt mit den gleichen fremden Strukturen zu einer stärkeren und vor allem schnelleren Reaktion fähig sind, ein Effekt, der z.B. bei der Schutzimpfung erwünscht ist. Man sagt, der Körper ist gegen ein bestimmtes Agens (Antigen) sensibilisiert. Dabei ist es unbedeutend, ob der Auslöser Viren, Proteine aus einem Blütenpollen oder individualspezifische Transplantationsantigene aus einem Organ sind.
Durch Bluttransfusionen, insbesondere Vollblut, durch Schwangerschaften oder durch vorangegangene Transplantationen können Patienten gegen Transplantationsantigene des MHC sensibilisiert werden. So sind sensibilisierte Transplantatempfänger Risikopatienten. Obwohl vor der Transplantation ein Kreuztest zwischen Empfängerserum und Zellmaterial des vorgesehenen Spenders durchgeführt wird – der natürlich negativ ausfallen muß – bleibt die große Unbekannte das immunologische Gedächtnis an frühere Immunisierungen durch Bluttransfusionen, Schwangerschaften oder vorherige Organtransplantationen.
TODO: Hier muss noch ein Bild rein

Große internationale Studien an Tausenden von Fällen (Abb. 43) zeigen eindeutig, daß diese „Präsensibilisierung“ einen starken negativen Einfluß auf das Transplantatschicksal nimmt. Insbesondere wiesen Patienten nach wiederholten Transplantationen (Retransplantationen) eine deutlich höhere Rate an Transplantat-Frühversagern gegenüber Ersttransplantationen auf, offensichtlich bedingt durch den Kontakt mit den fremden Antigenen des vorangegangenen Organspenders (vgl. Abschnitt „Transfusion und Transplantation“).
Obwohl nicht auszuschließen ist, daß es sich bei den nachweislich sensibilisierten Patienten um eine Gruppe von Individuen mit speziellen Respondereigenschaften handelt, die angeboren sind und einen genetischen Hintergrund haben, ist anzunehmen, daß es sich hier eher um eine immunologische Konditionierung – eben die Sensibilisierung – der Patienten handelt, die erst im Verlaufe des Lebens erworben wurde.
Zum Themenkreis „Individuelle Reaktivität“ kann man auch all jene Phänomene zählen, die mit dem Begriff „Allergie“ verbunden sind, wobei es sich bei der Allergie um eine Mischform aus angeborener Disposition und den Phänomenen der Reaktivierung eines sensibilisierten Zustandes handelt. Allein der Begriff drückt bereits die Tatsache aus, daß es sich hierbei um eine Andersartigkeit zu reagieren handelt. Warum einzelne Personen eine Sensibilisierung entwickeln, hängt von mehreren Umständen ab. Wichtige Faktoren sind die genetische Veranlagung, aber auch Umwelteinflüsse, die Ernährung oder bestimmte psychische Situationen.
Bei den Allergien handelt es sich um eine überschießende Reaktion des Immunsystems gegen körperfremde Substanzen der Umwelt. Auslöser (Allergene) können grundsätzlich fast alle meist hochmolekularen Stoffe unserer Umwelt sein, natürliche wie synthetische. Etwa 20.000 von ihnen sind bis heute bekannt.
Der Begriff Allergie ist an das Auftreten von spezifischen Immunreaktionen (Sensibilisierung) gebunden, die gegen Strukturen des immunisierenden Allergens gerichtet sind. Die Bildung von Antikörpern erfolgt meist erst nach Mehrfachkontakt mit dem Allergen. Bei der Allergie vom Soforttyp führt die Reaktion des Antikörpers mit dem Allergen zu einer überschießenden Ausschüttung von pharmakologisch wirksamen Substanzen (z.B. Histamine) aus speziellen weißen Blutzellen (Mastzellen) und den entsprechenden Krankheitssymptomen. Angaben über die Zahl von Nahrungsmittelallergikern schwanken stark. Für Erwachsene wird mit 1-5% gerechnet, bei Kindern unter sechs Jahren mit 3-10%. In Mitteleuropa sind am häufigsten Allergien gegen Erdnuß, Soja, Kuhmilch, Hühnerei, Fisch, Nüsse, Krustentiere und Sellerie zu beobachten. Nahrungsmittelallergien sind weniger häufig als Pollenallergien.
| Allergen | Kreuzreagierende Lebensmittel |
|---|---|
| Gräserpollen | Getreide-Mehle; Erdnuß; Soja |
| Frühblüherpollen | Apfel (besonders grünschalige Sorten); Aprikose; Erdbeere; Kirsche; Pflaume; Haselnuß; Mandel; Kartoffel (roh); Paprika; Tomate; Anis; Karotte; Kümmel; Sellerie; Fenchel; Koriander |
| Beifußpollen | Anis; Karotte; Kümmel; Sellerie; Fenchel; Kamille; Curry; Ingwer; Muskat; Pfeffer; Tomate; Paprika |
| Latex | Avocado; Banane; Kiwi; Kartoffel (roh); Tomate; Kastanie; Ficus benjamina (Birkenfeige) |
Wenn das auslösende Allergen in verschiedenen Quellen vorkommt, spricht man von Kreuzallergien (Tab. 17). Für die Betroffenen sind Kreuzallergien vor allem deswegen problematisch, weil die auftretenden allergischen Reaktionen nicht eindeutig auf ein bestimmtes Produkt oder eine Substanz zurückgeführt werden können. Hier liegt auch eine der Gefahren, die mit der Einführung bestimmter Gene in Nahrungsmittel verbunden ist. Zu den gut untersuchten Beispielen gehört die Einführung eines Gens der Paranuß in das Genom der Sojabohne mit dem Ziel, das Fehlen eines Methionin und Zystein enthaltenen Proteins in der Sojabohne zu kompensieren. Für Patienten, die gegen Allergene der Paranuß sensibilisiert sind, besteht dadurch bei Genuß dieser Sojaprodukte ein erhöhtes Risiko, für Paranüsse allergische Reaktionen zu entwickeln.
Andererseits gibt es ernstzunehmende Experimente, allergieauslösende Proteine aus Nahrungsmitteln durch Genmanipulation zu entfernen. So gibt es mehrere Untersuchungen, glutenfreien Weizen zu züchten. Damit könnte Menschen geholfen werden, die an einer allergischen Darmkrankheit leiden, die durch einen Bestandteil des Weizens (Gluten, Kleber), verursacht wird.
„Echte“ Allergien, die an die Beteiligung des Immunsystems gebunden sind, werden häufig mit Pseudoallergien und Intoleranzen (Unverträglichkeiten) verwechselt. Bei letzteren treten zwar ähnliche Symptome auf, aber es werden keine Produkte der Immunantwort gebildet. Bei der Pseudoallergie sind es bestimmte, in den Lebensmitteln enthaltene Botenstoffe, die eine Histaminausschüttung auslösen. Beispiele: Glutaminsäure (E620), Benzoesäure (E210), Sorbinsäure (E200). Anders als die Symptome bei Allergien sind pseudoallergische Reaktionen oft dosisabhängig. Daher können betroffene Personen wiederholt geringe Mengen des jeweiligen pseudoallergischen Stoffes zu sich nehmen, ohne daß Krankheitssymptome auftreten.
Intoleranzen haben ebenfalls mit den Allergien nichts gemein. Bei ihnen handelt es sich auch nicht um überschießende Reaktionen gegen ein definiertes Antigen. Bekannte Beispiele sind die Laktoseintoleranz (Milchunverträglichkeit) oder die Glutamatunverträglichkeit (das China-Restaurant-Syndrom). Ursachen für die bei Intoleranzen auftretenden Reaktionen auf einzelne Nahrungsmittel sind angeborene oder erworbene Enzymdefekte. Dadurch können anfallende Stoffwechselprodukte oder Nahrungsbestandteile nicht oder nicht ausreichend verdaut werden.
Fazit: Offensichtlich ist die Art und Weise, wie der Körper auf einen fremden Antigenreiz reagiert, u.a. an die genetische Ausstattung eines Individuums gebunden. Sie kann aber auch im Verlaufe eines Individuallebens erworben werden. Bei vielen Infektionskrankheiten findet bei der Erstinfektion eine Grundimmunisierung mit Bildung spezifischer Gedächtniszellen statt. Bei weiteren Infektionen mit den gleichen Keimen kommt es zu einer schnelleren und stärkeren Reaktion des Immunsystems. Dieses Phänomen wird bei Schutzimpfungen genutzt und ist z.B. bei wiederholten Organtransplantationen ein Risiko für den Transplantationserfolg.
