Bevor wir zur Besprechung eines der umstrittensten bioethischen Themen kommen, die gleichermaßen öffentliches Interesse, ernste Befürchtungen wie grundsätzliche Kritik hervorgerufen haben, soll über einige Fakten berichtet werden, die dazu geeignet sind, die persönliche Einstellung des Lesers zu diesem kontroversen Thema zu qualifizieren. Hinsichtlich der biologischen also auch molekularen Individualität ist das Thema dazu geeignet zu hinterfragen, ob es sich beim Klonen tatsächlich um das exakte Kopieren einer biologischen Vorlage handelt oder vielmehr um die Schaffung eines dem Vorbild nur ähnlichen Produkts mit wünschenswerten Eigenschaften. Urteilen Sie selbst.
Die allgemeine Definition lautet: Klonen ist die Herstellung eines genetisch gleichen Nachkommens von Pflanzen, Tieren oder Menschen. Der Begriff hat seinen Ursprung im griechischen Wort für „Sprößling“ oder „Zweig“. Auch in der Natur finden wir Zellklone. So sind eineiige Zwillinge Abkömmlinge einer befruchteten Eizelle als auch Bakterien, die sich bekanntlich durch Zellteilung vermehren, Klone eines Ausgangsorganismus‘.
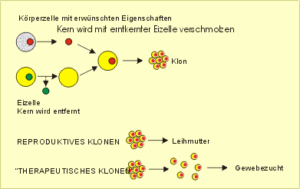
Es werden zwei Arten des Klonens unterschieden: das reproduktive Klonen und das sogenannte therapeutische Klonen (Abb. 57). Beim reproduktiven Klonen, wird der Zellkern aus einer ausdifferenzierten Körperzelle eines Tieres entnommen, dessen Eigenschaften vermehrt werden sollen. Dieser Kern wird in eine unbefruchtete Eizelle eines anderen Tieres eingepflanzt, deren Zellkern vor dieser Manipulation entfernt wurde. Nach kurzzeitiger Bebrütung in einer Nährlösung wird der Embryo wie bei einer normalen Schwangerschaft im Uterus einer hormonell „synchronisierten“ Leihmutter ausgetragen.
Die Idee dabei ist, daß die kernlose Eizelle für den eingepflanzten Kern mit den erwünschten genetischen Eigenschaften ein Milieu schafft, das alle Aktivitäten des Kerns auf das Niveau einer embryonalen Zelle „herunterregelt“ und die Individualentwicklung „von vorn“ beginnen läßt – übrigens ein sehr anschauliches Beispiel für die Abhängigkeit der Genexpression von ihrem jeweiligen molekularen Umfeld. Das Klonen ist ein mühseliges Geschäft. Hunderte von fehlgeschlagenen Versuchen sind erforderlich, um ein lebensfähiges geklontes Individuum zu erzeugen. Selbst in erfolgreichen Fällen werden oft Mißbildungen und ernsthafte Veränderungen des Stoffwechsels beobachtet.
Aber was macht das Klonen so stark vom Zufall abhängig? Man muß sich vor Augen führen, daß es sich um ein gewaltiges Umprogrammierereignis handelt. Das übertragene Kernmaterial muß „vergessen“, daß seine Aktivitäten auf die Funktion einer ausdifferenzierten Zelle programmiert waren. Wenn auch das neue Milieu der Eizelle einen wichtigen Einfluß auf die spätere Expression der Gene hat, so werden darüberhinaus mit dem eingefügten Kern auch regulierende Faktoren – z.B. die bereits oben erwähnten prägenden Histone und Methylketten an den DNS-Strängen aus der ausdifferenzierten Zelle des Kernspenders mit übertragen. Und die entkernte Eizelle ist zwar kernlos, besitzt ansonsten aber alle restlichen „Inhaltsstoffe“ und Organelle einer Zelle, die Einfluß auf die DNS des importierten Zellkerns nehmen können. Besonders hervorzuheben sind vor allem die Mitochondrien, die – wie bereits berichtet – wichtige genetische Informationen tragen und beim Menschen etwa 1% der genetischen Information ausmachen (vgl. Abschnitt „Das Mitochondriengenom“).
Spätestens an dieser Stelle erhebt sich die Frage nach der Präzision des Klonens: Wie identisch ist das Klonprodukt gegenüber seinem Original oder wie gleicht das eine Individuum dem anderen? Offensichtlich zeigt die Tatsache, daß das erfolgreiche Klonen von vielen gleichzeitigen biologischen und labortechnischen Bedingungen und Einflüssen abhängt und das komplexe molekulare Umfeld nach dem Kerntransfer kaum völlig zu beherrschen ist.
Das Verfahren des Klonens geht auf eine Idee des deutschen Nobelpreisträgers Hans Spemann (1938) zurück, die in der Geburt des ersten geklonten Tieres im Jahre (1986) mündete, allerdings noch mit einem Kern aus einer embryonalen Zelle. Auf diesem Prinzip beruht u.a. auch die Schaffung des ersten vaterlosen Klonschafs namens „Dolly“ in England (5. Juli 1996) unter Verwendung eines (diploiden) Kerns einer ausdifferenzierten Euterzelle und des am 23. Dezember 1998 in München geborenen ersten deutschen geklonten Kuhkalbs „Uschi“.
Seither existiert eine ganze Reihe geklonter Tierarten. Einerseits ist beabsichtigt, auf diese Weise Zuchttiere zu schaffen, die resistent gegen bestimmte Krankheiten wie Tuberkulose, Brucellose oder Salmonellose sind, andererseits Tierarten zu retten, die im Aussterben begriffen sind wie im Fall des Tasmanischen Tigers oder des Riesenpandas. Zu den bisher mehr oder weniger erfolgreich geklonten Tierarten gehören sowohl edle Rassen von Hunden und Katzen sowie Labortiere wie Ratten und Kaninchen als auch Pferde, Kühe und Schweine. Letztere könnten, wie bereits erwähnt, besondere Bedeutung im Zusammenhang mit Befriedigung der riesigen Nachfrage nach Spenderorganen im Rahmen der Organtransplantation erlangen (vgl. Abschnitt „Transplantation und Transfusion“).
Und wie steht es um das Klonen von Menschen? Das Klonen eines Menschen ist in vielen Ländern verboten: Bereits die Ankündigung eines solchen Vorhabens wurde von der Deutschen Forschungsgemeinschaft sofort als unmoralisch, von US-amerikanischen Forschern als kriminell verurteilt. Ein Zusatzprotokoll zur Europäischen Bioethik-Konvention verbietet ebenfalls das Klonen von Menschen ohne Ausnahme mit der Begründung, daß „die Instrumentalisierung der Menschen durch die willentliche Erschaffung von genetisch identischen Menschen im Gegensatz zur menschlichen Würde steht und daher einen Mißbrauch der Biologie und Medizin darstellt“. Die Klonierung von menschlichem Zellmaterial für therapeutische Zwecke befindet sich noch weitgehend im Stadium der Grundlagenforschung.
Das Prinzip des therapeutischen Klonens ähnelt sehr dem Vorgehen beim reproduktiven Klonen: Ein Kern aus einer ausdifferenzierten Körperzelle wird in eine „entkernte Eizelle“ gebracht und unter Kulturbedingungen weitergezüchtet, also nicht wie beim reproduktiven Klonen in einem weiblichen Organismus in den Uterus eingebracht. In einem sehr frühen Stadium der Embryonalentwicklung (beim Menschen etwa bis zum 8-Zellstadium), wenn noch keine Differenzierung der Zellen stattgefunden hat, wird der kleine Zellhaufen geteilt und jede Einzelzelle weitergezüchtet.
Zu diesem Zeitpunkt sind die Zellen noch totipotent. Dies bedeutet, daß sich aus jeder Einzelzelle ein vollständiger Organismus entwickeln könnte. Beim therapeutischen Klonen werden also Embryonen zerstört, um aus ihnen die sog. embryonalen Stammzellen zu gewinnen. Letztere bilden wiederum die Grundlage dafür, um daraus in Zukunft Gewebe und (in noch fernerer Zukunft) beliebige Organe zu züchten, die therapeutisch eingesetzt werden könnten – daher der Name therapeutisches Klonen – der besser heißen sollte: Klonen zu therapeutischen Zwecken. Kritiker vermuten hinter dem assoziierten Begriffsbild nur eine Verschleierung der Tatsache, daß es sich um das Töten früher Embryonen handelt, unabhängig von der Zeugungsart (In-vitro-Fertilisation [IVF], der intrazytoplasmatischen Spermieninjektion [ICSI] oder durch Klonen).
Alternative Wege sind bereits beschritten worden, um Stammzellen zu gewinnen, ohne daß ethische Bedenken ausgeräumt werden müssen. Als erste sollen hier die „adulten Stammzellen“ genannt werden. Dabei handelt es sich um Stammzellen aus dem Körper ausgereifter (adulter) Individuen, wie wir sie bereits im Zusammenhang mit der Knochenmarktransplantation kennengelernt haben. Diese Zellen sind hinsichtlich ihrer Differenzierungsmöglichkeiten zwar eingeschränkt, also nicht totipotent, wie die frühen embryonalen Stammzellen. Sie besitzen jedoch noch die Qualität, sich in Gegenwart verschiedener Wachstumshormone in vivo oder in vitro zu spezialisierten Zellen (z.B. Nerven- oder Muskelzellen) zu entwickeln. Gewinnt man diese Stammzellen z.B. in der Remissionsphase der Leukämie aus dem Körper des zu behandelnden Patienten und gibt sie nach entsprechender Manipulation im richtigen Moment in den Patienten zurück, so hat dies den entscheidenden Vorteil, daß der Stammzellempfänger, da es sich um seine eigenen Zellen handelt, keine immunologischen Abwehrreaktionen entwickeln wird.
Fazit: Das Klonen hat das Ziel, viele Organismen mit gleichen erwünschten Eigenschaften zu erzeugen. Das Prinzip besteht in der Isolierung des Kerns einer ausdifferenzierten Körperzelle eines Organismus mit den erwünschten Eigenschaften und dem Einfügen dieses Kerns in die „entkernte“ Eizelle eines anderen Tieres. Hintergrund ist die Erwartung, daß das „Milieu“ der Eizelle die Gene des eingefügten fremden Zellkerns auf ein Niveau herunterregelt, das demjenigen einer gerade befruchteten Eizelle entspricht. Nach wenigen Teilungsschritten, wenn die Zellen noch zur Bildung aller möglichen Zelltypen für einen neuen Organismus fähig sind, wird der kleine Klon zum Austragen in eine „Leihmutter“ gegeben (reproduktives Klonen) oder der Klon zerteilt, um aus den Einzelzellen durch Zellzucht Gewebe oder Organe zu gewinnen („therapeutisches Klonen“). Neben ethischen Bedenken gibt es prinzipielle biologische Schwierigkeiten beim Klonen, die in der Rückprogrammierung des Genoms aus der ausdifferenzierten Zelle und dem Einfluß des Zellplasmas und dem genetischen Material der Mitochondrien der Eizelle bestehen.
