Am Beispiel der Immunzellen werden wir später erfahren, daß sie als pluripotente Zellen (Stammzellen) aus dem Knochenmark stammen, unter dem Einfluß bestimmter Zellhormone reifen und so zur Erkennung fremder Strukturen z.B. an Bakterien und Viren befähigt werden. Die auf diese Weise immunkompetent gewordenen Zellen – hauptsächlich noch ungeprägte T-Lymphozyten und vor allem Gedächtniszellen mit ihrem Erinnerungspotenzial an ihren Erstkontakt mit immunologisch Fremdem – durchstreifen alle Gewebe, um körperfremde molekulare Strukturen aufzuspüren. Sie wandern über die Lymphbahnen in die Lymphknoten bzw. über den Blutkreislauf in die Milz, wo in separaten Bereichen die eigentliche primäre Antigenpräsentation stattfindet (Homing im engeren Sinne). Dort vermehren sich dann jene Zellen, die spezifisch gegen die als fremd erkannten Strukturen gerichtet sind. Sie bilden aktivierte Immunzellen, die selbst oder durch die Bildung spezifischer Antikörper die Immunattacke gegen das molekular Fremde ausführen können.
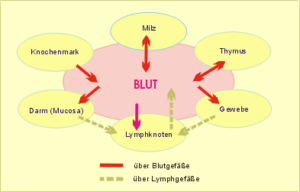
Über die Blutbahn gelangen sie dann wieder genau an den Ort, an dem sie gebraucht werden. Dort müssen die Immunzellen die feinen Blutgefäße verlassen, um in das Gewebe eindringen zu können und dort gezielt ihre Funktion – nämlich die Neutralisierung oder Eliminierung des Fremden – im Zusammenwirken mit anderen Zellen zu erfüllen. Der letzte Abschnitt der Zellwanderung führt sodann zurück zu den Ursprungsorganen, wo der Abbau der gealterten Zellen stattfindet.
An der beschriebenen Rezirkulation nehmen etwa 80% der im Blut kreisenden Lymphozyten teil. So zirkuliert pro Stunde etwa 1 % der Lymphozyten durch die Gewebe und die kontrollierenden lymphatischen Organe Milz und Lymphknoten. Abb. 30 vermittelt einen Eindruck von den Wanderungswegen der Immunzellen. Sie legen auf ihrer Reise gewaltige Entfernungen zurück und steuern wie die Zugvögel erstaunlich genau ihr Ziele an. Wie aber finden nun die Immunzellen ihren Weg von Ort zu Ort? Kann man dafür spezifische Moleküle benennen?
Bewegende mechanische Kraft ist natürlich der Blutstrom bzw. der weit langsamere Fluß in den Lymphgefäßen. Wo die zirkulierenden Immunzellen „hängen bleiben“ ist von der Ausstattung der Zellen mit einer bestimmten Gruppe von Oberflächenmolekülen, sog. Adhäsionsmolekülen auf ihrer Zellmembran abhängig. Zu jedem Molekül (Rezeptor) paßt ein Gegenmolekül (Ligand) (Schlüssel-Schloss-Prinzip). Interessanterweise gehören diese Moleküle (Selektine, Integrine, Adhärine) genetisch und molekular betrachtet zur Immunglobulin-Superfamilie, zu denen auch die spezifischen Antikörper gehören. Im Gegensatz zu den „richtigen“ Immunglobulinen (Antikörpern) sind ihre Gegenmoleküle nicht Eiweiße, sondern ausnahmslos Zuckermoleküle und deren Abkömmlinge. Insofern ähneln sie sehr den Lektinen, die bei Pflanzen und entwicklungsgeschichtlich niederen Lebewesen wesentlich zur Selbst-Fremd-Unterscheidung und Fremdabwehr beitragen .
Trifft also eine zirkulierende Zelle mit einem bestimmten Liganden während ihrer Reise auf einen entsprechenden komplementären Rezeptor, so hat sie ihren Zielort gefunden. Durch die Interaktion von Rezeptor und Ligand werden Reaktionen ausgelöst, die unter anderem zur An- und Abschaltung bestimmter Gene führen, was u.a. die Freisetzung einer Reihe von Signalstoffen bewirkt und sich z.T. dramatisch auf das Molekülmuster an der Zelloberfläche auswirken kann. Durch die so erzeugte neue Ausstattung der Zellmembran mit anderen Molekülen ergibt sich für die so modifizierte zirkulierende Zelle die Möglichkeit, ihr nächstes Ziel zu finden. Auf diese Weise wird ein mehrstufiges Homing erzielt und die gerichtete Zirkulation in Bewegung gehalten.
Dieses molekulare Prinzip ist an allen Prozessen beteiligt, wo es darauf ankommt, „daß zusammenkommt, was zusammengehört“. Es trägt dabei beträchtlich zur anatomischen und funktionellen Selbstorganisation des Organismus bei. Zwei Beispiele sollen das Prinzip verdeutlichen:
Knochenmarktransplantation. Bei der Knochenmarktransplantation werden in der Regel dem Patienten Stammzellen eines gesunden Spenders übertragen, die im Empfänger zum Knochenmark wandern sollen, um dort die Produktion neuer, gesunder Blutzellen aufzunehmen.
Die Stammzellen des Spenders werden in die Blutbahn des Empfängers infundiert. Manche Transplantationen scheitern jedoch daran, daß zu wenig Stammzellen vom Blutkreislauf in das Knochenmark gelangen. Ursache ist, daß sich in diesen Fällen die meisten Stammzellen bereits zu roten und weißen Blutzellen ausdifferenzieren und sich nur wenige Stammzellen im Knochenmark einnisten, um sich dort zu vermehren und als Reservoir für eine geregelte Blutbildung zu dienen. Israelische Wissenschaftler haben an Mäusen herausgefunden, daß die übertragenen Stammzellen an ihrer Zelloberfläche zu wenige Moleküle eines Rezeptors (CXCR4 ) aufweisen, der in der Lage ist, bestimmte Signalmoleküle der Knochenmarkzellen zu identifizieren, die dafür sorgen, daß die übertragenen Stammzellen auch wirklich in das Knochenmark gelangen. Der therapeutische Ansatz besteht nun darin, die zu übertragenden Stammzellen so zu konditionieren, daß sie eine ausreichende Anzahl von Rezeptoren an ihrer Zelloberfläche exprimieren, um ihre Gegenmoleküle im Knochenmark zu finden. Ein erster Schritt könnte auch sein, Knochenmark vor der Infusion hinsichtlich der Rezeptorbildung zu untersuchen und nur geeignetes Spendermaterial zu verwenden.
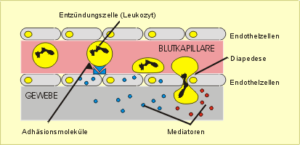
Entzündungsreaktion. Eines der charakteristischen Merkmale der Entzündungsreaktion ist das Auswandern von weißen Bluzellen aus der Blutbahn in das betroffene verletzte oder infizierte Gewebe (Abb. 31). Bestimmte Adhäsionsmoleküle – sog. Selektine – an der Oberfläche der die Blutkapillaren auskleidenden Endothelzellen erkennen spezifisch bestimmte Zuckermoleküle an der Oberfläche von weißen Blutzellen. Dies führt zu einer komplexen Kaskade von Adhäsionsereignissen. In deren Gefolge kommt es zu einer Verlangsamung der fließenden Leukozyten im kapillaren Blutstrom und zu einer lokalen Konzentration der Leukozyten. Die bei diesem Prozeß freigesetzten Mediatoren (Botenstoffe) lockern die Zell-Zellverbindungen der Endothelzellen und ermöglichen auf diese Weise den Durchtritt der Leukozyten aus der Blutbahn in das Gewebe (Diapedese). Auf diese Weise können die Leukozyten zu ihrem Wirkort gelangen und eventuelle Keime neutralisieren oder vernichten.
Adhäsionsmoleküle spielen heute als Zielstruktur in der pharmazeutischen Forschung eine bedeutende Rolle. Dabei geht es vor allem darum, bei Erkrankungen, die mit pathologischen Entzündungsprozessen wie z.B. beim Rheuma, der Schuppenflechte oder dem Morbus Crohn das Bindungsvermögen der Adhäsionsmoleküle mit geeigneten Medikamenten zu dämpfen oder zu blockieren.
Fazit: Unter Homing versteht man das „Nachhausefinden“ verschiedener im Körper zirkulierender Zellen zu ihren Wirkorten. Im engeren Sinne ist damit das Auffinden der Orte der Antigenpräsentation in den lymphoiden Organen durch die Immunzellen (T-Lymphozyten) gemeint. Das Auffinden dieser Orte wird durch verschiedene komplementäre molekulare Strukturen vermittelt.
